[연재 기고] 인공지능화된 나노 바이오센서 기술이 보여주는 세상
2024-01-03 고려대학교 주병권 교수님 연구실
나노 기술을 이용한 바이오 센서
바이오센서(biosensor)는 1960년대 효소 전극을 이용한 포도당을 감지한 글루코즈 센서 개발을 시작으로 1990년대 후반까지는 주로 임상적인 수요가 큰 혈당 센서에 집중되어 왔으나, 최근 바이오(BT), 정보통신(IT), 나노기술(NT), 환경 및 에너지 (ET) 등 기술간 융합으로 새로운 패러다임가능성을 보여주고 있다.
특히 급속도로 성장 중인 생명공학과 반도체 기술 기반의 IT 나노기술이 만난 NBIT 융복합 기술은 유전자 치료, 줄기세포 기술, 암 정복 등 여러 형태로 응용 발전하고 있다. 이 중 나노 바이오센서는 다양한 질병의 검사, 치료, 예후 모니터링이 필요한 임상진단 분야에서 비약적인 기술 개발 및 응용 가능성을 제시하고 있다.
.JPG)
글/ 고려대학교 주병권 교수님 연구실
주병권 (고려대학교 전기전자공학부 교수)
김기수 (고려대학교 전기전자공학부 박사 과정)
목차
1. 서론
2. FET 나노 바이오센서 원리
3. Debye 길이
4. 성능 향상을 위한 나노 재료 기술
4-1. SiNW (실리콘 나노와이어)
4-2. CNT (탄소 나노튜브)
4-3. Graphene (그래핀)
5. FET 나노 바이오센서 연구 동향
5-1. COVID-19 나노 바이오센서
5-2. 나노 바이오 전자 코
6. 결론
7. 참고 문헌
1. 서론
나노 바이오센서는 특정 물질에 인식/반응하는 바이오 탐침(bio-probe)이 전기/화학/광학적 변환기(transducer)와 결합하여 타깃 생물분자와의 상호작용을 통해 극미량의 생화학적 물질을 선택적으로 감지할 수 있는 소자를 뜻한다.
생물학적 탐침은 압타머(aptamer), 항원/항체(antigen), 수용체(receptor), 베지클(vesicle) 등이 있으며 변환기는 전도성 나노 구조체(CNT, 전도성 고분자, SiNW, 그래핀, TMD 등)와 형광 구조체(금속, 퀀텀닷), 나노 에너지 상향물질(up-conversion) 등이 있다(그림 1).

나노 바이오센서는 변환기 종류에 따라 크게 기계/광/전기화학/전기적 소자로 구분할 수 있으며(그림 2), 특히 전기적 신호를 감지하는 반도체 기술 기반 FET(전계유발효과 트랜지스터, Field-effect transistor)의 경우 소형화, 대량생산, 고민감도, 고속도 진단이 가능하다는 점에서 매우 큰 장점을 갖고 있다. 본 기고에서는 바이오센서 기술의 원리 및 다양한 나노 재료 기술을 이용한 고민감도/고속 검출 바이오센서 소자 개발에 대해 다루고자 한다.

2. FET 나노 바이오센서 원리
일반적인 반도체 센서 MOSFET은 소스(source), 드레인(drain), 게이트(gate)로 구성되어 있다. 이러한 구조에서 게이트에 양의 전압, 소스에 음의 전압이 걸리게 되면 표면전자 축적으로 N채널이 형성된다. 그러나 게이트와 소스 사이에 음의 전압이 걸리거나 전압이 걸리지 않을 경우 이 N채널은 사라지게 된다. 이렇게 선택적으로 형성되는 N채널을 통하여 소스와 드레인 사이 선택적으로 전류가 흐르기 때문에 게이트 전압은 소자 내 흐르는 전류를 제어하게 된다.
이와 유사하게 FET 나노 바이오센서는 전하를 띤 타깃 생물분자와 바이오 탐침이 결합할 때 표면 전위 변화가 발생될 수 있다. 이 전위 변화는 N채널을 형성하거나 소실시키는 기존 MOSFET에서의 게이트 전압 역할과 같으며 이로 인해 소스에서 드레인으로 흐르는 전류값 변화가 유도될 수 있다(그림 3).
 그림 3. FET 소자와 FET 나노 바이오 소자의 구조 비교
그림 3. FET 소자와 FET 나노 바이오 소자의 구조 비교
바이오센서의 검출 동작은 3단계로 구성된다. 첫째, 타깃 생물분자를 인지하는 단계로써 생물분자의 농도에 따른 전도도의 변화값을 유도한다. 둘째, 바이오 탐침이 인지한 전기적 성질 변화가 전기적 신호로 전환된다. 셋째, 전환된 전기적 신호를 증폭하여 데이터로써 처리한다 (그림 4).
이 때 타깃 생물분자는 나노 전도성 물질(채널)까지 확산 이동 후 화학적/물리적 흡착(반데르 발스 힘)을 하게 되며 이로 인해 전환되는 전기적 신호는 전도도 변화, 문턱전압 변화, 유도되는 전류값의 변화를 의미한다.

반도체 소자인 FET의 종류와 흡착되는 타깃 생물분자의 전하 종류에 따라 그림 5와 같은 형태로 전류값의 변화가 발생된다.
또한 그림 6에서 보는 바와 같이 문턱 전압이나 전도도 값의 변화로 검출 신호를 읽을 수도 있다.

 P타입 CNT 기반 FET 나노 바이오센서의 특성, (b) 문턱전압 변화, (c) 전도도 변화.jpg)
3. Debye 길이
FET 바이오센서는 전해질이 존재하는 용액 내 반도체 소자가 담겨 있는 형태로 작동한다. 따라서 이온 농도가 높은 용액 속에서 동작을 하게 된다면 용액 속의 이온이 전기적 신호를 상쇄(neutralization)시킴으로써 FET의 전기적 변화 측정이 어려워질 수 있다.
이러한 전기적으로 차폐되는 정도를 표현하는 개념을 Debye 길이라고 하며, 전하를 띠고 있는 입자가 영향을 미치는 거리를 의미한다. Debye 길이에 대한 Helmholtz, Gouy, Chapman, Stern 등 다양한 모델이 제시되어 왔으며 결론적으로 Debye 길이 K는 이온의 농도가 증가할수록 감소하게 된다 [5], [6].
즉, 이온 농도에 따라 결정되는 전하간 유효거리인 Debye 길이는 고농도 이온에 의한 중성화로 전기적 시그널이 약화되어 FET 바이오센서의 민감도가 저하될 가능성이 높아 기능적인 설계가 요구된다(그림 7). 이러한 문제를 해결하기 위해 바이오 탐침 길이 감소(인공항체, 앱타머 등), 저농도 용액 사용, 용액 탈양성자화 및 PH 증가, 고주파 처리법 등 다양한 연구가 적용되고 있다.

4. 성능 향상을 위한 나노 재료 기술
기존의 박막 형태의 FET 바이오센서의 경우 박막 트랜지스터 표면과 타깃 생물분자간 반응을 통한 트랜지스터 전류 변화를 측정하는 방식이었지만, 이러한 박막 트랜지스터의 경우 크기가 작아지면 반응 표면적이 감소하여 센서의 민감도가 급격하게 떨어진다는 단점을 갖고 있었다.
따라서 박막을 반응 표면적이 넓은 나노 물질로 대체함으로써 고민감도 초소형 바이오센서를 제작할 수 있다는 가능성이 제기되었다. 이는 생체분자의 작은 크기가 나노 구조체와 유사하다는 점과 나노 물질의 부피당 생체분자와 결합할 수 있는 표면적이 크게 향상되기 때문이다 (그림 8).
또한 나노 물질 재료 자체의 높은 전기전도도 및 전하 이동도를 통해 센서 성능 지표인 검출 한계(LOD, Limit of detection)을 개선시킬 수 있다 [7]. 추가적으로 나노 물질의 형상 및 구조 변경과 나노 물질의 화학적 표면 기능화를 통해 다양한 연구 활동이 진행되고 있으며, 본 고에서는 최근 가장 활발히 발표되고 있는 대표적인 나노 물질에 대해서 다뤄보고자 한다.

4-1. SiNW (실리콘 나노와이어)
SiNW는 일반적으로 랜덤한 방향과 직경 길이로 성장하지만 성장 방법 및 공정을 조절하여 다양한 형태로 제어 가능하다. 따라서 SiNW의 전기적 특성은 성장 방향, 직경, 표면 개질, 도핑 및 와이어의 정렬 방향에 영향을 받게 된다. 예를 들어 SiNW의 밴드갭은 나노와이어의 직경에 반비례한다. 또한 2011년 Ramanujam 그룹에서는 SiNW의 전하 이동도(Charge mobility)와 합성 및 구조와의 관계를 이론적 모델과 실험 결과를 통해 밝힌 바 있다 [8]. 캐리어 이동성은 도핑, 열처리 및 산화물 결함의 패시베이션에 의해 개선됨을 보고한 바도 있다.
일반적으로 실험 결과를 통해 SiNW의 직경, 길이, 개수가 감소할수록 센서의 민감도 및 감지속도가 빨라지는 경향을 보였으며, 단위 부피당 표면적비 증가를 통한 표면 전하 효과와 전자 이동속도 증가와 관계된다고 확인되었다.
직경이 20 nm로 작은 SiNW의 경우 열처리 공정을 통해 최대 103 cm2V-1s-1 수준의 전하 이동도를 보이며, 직경이 5 nm 이하로 형성된 경우 전자와 홀의 이동도는 약 325 cm2V-1S-1와 750 cm2V-1s-1 수준까지 확인되었다. 또한 SiNW 나노 물질은 높은 전류 on/off 비, 낮은 누설전류 특성은 물론 도핑, 표면, 와이어 디자인을 설계함으로써 다양한 전기적 특성을 제어할 수 있다는 점에서 나노 바이오센서 재료로 선호되고 있다.
SiNW 나노 물질은 고가이지만 정확하고 균일한 합성과 패터닝이 가능한 Top-down (하향식) 리소그래피와 저가 대량 생산이 가능하지만 불균일한 합성이 이루어지는 Bottom-up (상향식) 기체-액체-고체(VLS) 공법을 통해 제조가 가능하다. 최근에는 보다 진보된 나노 임프린트 기술을 이용하여 대량 생산 가능하면서도 균일한 SiNW 구조를 형성시키는 신규 공법이 소개되고 있다(그림 9).
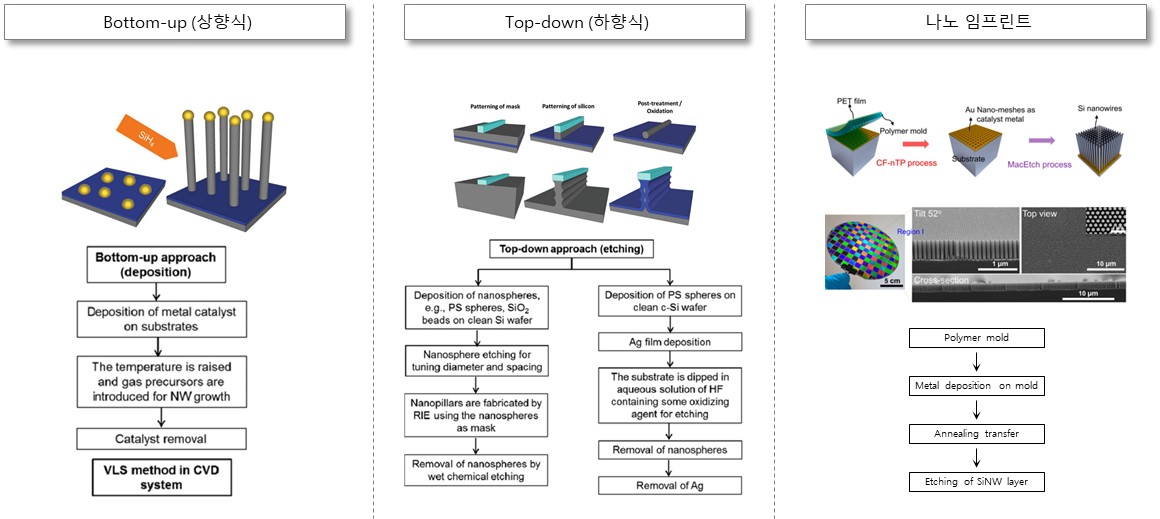

그림 10. SiNW가 형성된 FET 소자의 SEM 이미지 [10]
4-2. CNT (탄소 나노튜브)
CNT는 6개의 원자로 이루어진 고리로 탄소 간 결합은 sp2 구조를 갖는다. 이 그래핀 시트 (graphite sheet)가 원통형으로 말려 있는 구조로 카이랄(말림) 지수에 따라 전기적 특성은 반도체 및 도체의 특성으로 구분될 수 있으며 구리의 103배(~10^7 S/m)의 매우 높은 전기전도도(~3,500 W/mK)와 다이아몬드 수준의 열전도도를 갖게 된다. CNT는 직경이 1~30 nm, 길이는 수~수백 um로 매우 높은 종횡비를 가지며 넓은 표면적(50~1,315 m2/g)으로 센서 감도를 향상시킬 수 있다는 장점을 갖는다.
또한 금속보다 우수한 100 GPa 수준의 인장강도와 수 TPa 수준의 탄성계수를 갖고 있기 때문에 유연성 소자로도 적용이 용이하기 때문에 FET 나노 바이오센서로 매우 적합한 나노 물질이다.
 SWCNT의 다양한 카이랄 특성, (b) 다양한 카이랄 특성으로 구성된 MWCNT 구조.jpg)
이러한 CNT 나노 물질은 FET 나노 바이오센서에 적용하기 위해 필름의 형태로 제작하여 소자에 전사하게 된다. 우선 CNT를 성장시킨 후 정제, 분산, 분리, 도핑 등의 공정이 필요하다.
CNT는 아크 방전, 레이저 열처리, 화학기상증착(CVD) 등을 통해 성장시킨 후 카본계 불순물 및 촉매 금속 불순물 등을 제거하기 위한 산 처리와 고온 열처리를 통해 정제를 함으로써 보다 고순도의 CNT를 얻어 낼 수 있다. 이후 CNT간 반데르발스 힘으로 결합된 번들을 분리하기 위해 볼밀링, 초음파 처리, 계면활성제, 화학적 산화처리를 통해 분산을 시키게 된다. 이렇게 형성된 CNT는 앞서 설명한 바와 같이 카이랄 특성으로 인한 반도체성과 금속성이 혼재되어 있는 상태이기 때문에 밀도차이를 이용한 초원심분리기나 칼럼 크로마토 공정을 통해 선택적으로 분리가 필요하다.
마지막으로 확산로를 통한 합성 혹은 도펀트가 포함된 폴리머를 이용하여 전자를 공급함으로써 CNT의 전기적 특성을 조절할 수 있다. 이렇게 형성된 CNT는 딥 코팅, 스프레이 코팅, 잉크젯 코팅 등 다양한 방법을 통해 소자 위에 전사함으로써 CNT 기반 FET 나노 바이오센서를 제작하게 된다(그림 12).
이렇게 제작된 FET 바이오센서의 경우 CNT의 우수한 물성으로 인해 전기 전도성이 우수하고, 고집적도, 저전력, 빠른 스위칭 속도 등의 장점을 가지고 있으나 CNT 배열, 카이랄 특성 기인 도체/반도체성 CNT 분리, CNT 특성 균일도, 전극/CNT간 오믹컨택 등의 물성 및 공정 이슈가 존재하여 향후 개선이 필요한 상황이다.

4-3. Graphene (그래핀)
그래핀은 탄소 동소체 중 하나로 탄소 원자들이 모여 sp2 공유결합으로 2차원 평면 구조를 이루고 있다. 각 탄소 원자들은 육각형의 격자를 이루며 육각형의 꼭지점에 탄소 원자가 위치하고 있는 모양이다. 그래핀은 실리콘의 100배 수준의 높은 전하 이동도와 높은 비표면적 (2,630 m2/g)을 갖고 있어 나노 센서로써 매우 우수한 민감도를 확보할 수 있는 물질이다.
또한 높은 열전도도(구리의 13배), 전류 밀도(구리의 100배) 및 내화학성, 기계적 강도, 유연성, 투명성의 장점도 갖고 있다. 하지만 물질 내부에 밴드갭이 없는 제로 밴드갭 특성으로 인해 인위적 도핑 공정이 필요하고 이 과정에서 우수한 전기적 특성이 저해된다는 점과 낮은 전류 스위칭 비로 인해 센서 감도의 저하를 가져올 수 있다는 문제점도 있다. 소자를 제작하는 과정에서 그래핀의 산화도 발생할 수도 있다(그림 13).
따라서 이러한 이슈들을 개선해 나가기 위해 최근 그래핀 계면 및 결함 제어, 산화/ 환원 그래핀 기반 설계, 그래핀 폭을 좁게 만드는 나노 리본 구조 형성, 전류 채널을 새롭게 설계하는 기술 등이 제시되고 있다.
 특성 및 제로 밴드갭 형태의 그래핀 구조.jpg)
이러한 그래핀 나노물질은 FET 나노 바이오센서에 적용하기 위해 합성, 정제, 분산, 분리/전사 공정 후 도핑처리를 하게 된다. 그래핀을 제조하는 방식은 첫째, 흑연으로부터 그래핀을 만들어 내는 Top-down 방식과 둘째, 탄소원으로부터 그래핀을 화학적으로 합성하는 Bottom-up 방식이 있다.
구체적으로는 스카치 테이프를 이용하여 물리적으로 벗겨 내는 기계적 박리법 및 화학적 박리법, 화학기상 증착법(CVD 증착), 결정 성장법(Epitaxial growth) 등 다양한 방법들이 있으나 최근 고품질의 그래핀을 대량생산하는데 장점이 있는 화학기상 증착법을 개발하여 상용화 준비를 하고 있는 연구 기관 및 업체들이 나타나고 있다(그림 14).
마지막으로 이렇게 형성된 그래핀은 필름의 형태로 FET 나노 바이오센서 소자 위에 전사되는데 가장 대표적인 방식은 Ni이나 Cu 금속 호일 위에 성장/형성된 그래핀을 화학 에칭하여 전사하는 공정이라고 할 수 있다.

이와 같이 다양한 나노 재료와 구조들이 FET 나노 바이오센서에 적용되고 있으며 그림 15와 같이 각각의 특성과 연구방향을 정리해 보았다.

5. FET 나노 바이오센서 연구동향
5-1. COVID-19 나노 바이오 센서
최근 코로나 팬더믹 시대를 맞아 매우 다양한 바이러스 검출을 위한 센서 개발이 이뤄졌다.
이 중 한 예로써 높은 비표면적과 빠른 전자 이동도를 가진 그래핀 나노 물질을 FET 나노 바이오센서에 적용하여 COVID-19(코로나 바이러스)를 검출한 바 있다.
그래핀 시트에 COVID-19와 항원체와 특정 결합할 수 있는 항체를 코팅하고, 그래핀과 이 항체간 계면을 고정화하기 위해 계면 결합제(링커)로써 PBASE (1-pyrenebutyric acid N-hydroxysuccinimide ester)를 사용하였다. 이를 통해 COVID-19 감염 여부를 고민감도로 검출할 수 있었으며 센서의 성능 지표인 검출한계(LOD)가 약 펨토몰(~ fm) 수준으로 매우 높은 결과를 확인할 수 있었다(그림 16).
 COVID-19 검출용 FET 나노바이오 센서 플랫폼, (b) PBS내에서 COVID-19 항원에 대한 바이오 센서 검출 결과, (c) COVID-19 항원 주입량에 따른 결과값 (Vds = 0.01V), (d) COVID-19와 MERS-CoV 바이러스간 선택적 검출 반응.jpg)

5-2. 나노 바이오 전자 코 (Bioelectric-Nose)
전자 코는 냄새를 구성하는 화학물질을 정량적으로 센싱하고 감지하는 장치로써 바이오, 식품, 군사 산업 등 다양한 분야에 활용되고 있다. 1970년대부터 인간의 호기 가스(Breath gas)를 분석하기 위해 기술 개발이 시작되었으나, 수 백 가지 종류의 호기 가스를 선택적으로 민감하게 센싱하는데 극히 제한적이었다.
이러한 문제점을 극복하기 위해 최근에는 사람의 코를 모방한 나노 바이오 전자 코를 개발하고 있다. 사람의 코는 약 400여개의 바이오 탐침(후각 수용체)를 가지고 있으며 각각의 바이오 탐침들이 하나의 냄새 분자들과 선택적/특이적으로 결합함으로써 냄새를 지각하게 된다.
따라서 특정 냄새분자와 결합 가능한 바이오 탐침과 FET 나노 센서를 융복합함으로써 기존의 수백~수천 배가 넘는 센싱 민감도와 특이도를 확보할 수 있었다. 전자 코 또한 FET 나노 바이오센서와 같이 바이오 탐침(후각 수용체)와 특정 냄새분자가 결합될 때 형성된 게이트 전압의 값에 따라 트랜지스터 소자의 표면 전하량이 변화되는 원리를 따른다(그림 17).

탄소 나노튜브(CNT)를 FET 나노 센서에 적용하고, 바이오 탐침에 필요한 단백질체를 대장균 시스템을 통해 생산 후 CNT 채널에 고정화한 결과 화학적 구조가 유사한 특정 냄새 분자만을 선택적을 검출할 수 있었음을 확인하였다 (그림 18).
또한 MEMS 공정을 이용한 그래핀 마이크로 패턴된 FET 나노 바이오 센서를 제작하여 여러가지 종류의 냄새 분자를 동시다발적으로 측정하는 플랫폼 또한 보고된 바 있다. 이 연구에서는 특히 화학무기의 한 종류인 사린 가스(독가스) 감지를 위해 사린 가스와 유사한 구조이나 독성이 적은 디메틸 메틸포스포네이트(DMMP)로 대체하고, 바이오 탐침인 hOR2T7을 그래핀에 구조화하는 형태로 검출하였다. 이는 인체 단백질인 바이오 탐침이 안정적으로 타겟 냄새 분자와 결합할 수 있도록 세포막을 감싸고 지지하는 형태로 구조화함으로써 민감도와 특이도를 개선시킬 수 있기 때문이다(그림 19).
이와 같은 나노 바이오 전자 코 기술은 현재 화장품, 식료품 등에 적용되고 있는 상황이지만 향후에는 사람의 호흡 가스로부터 방출되는 질병(폐암, 유방암 등 암, 알츠하이머, 당뇨 등)이나 바이러스, 기타 마약류나 독성 가스 혹은 친환경(공기 질) 기술 등에 활발히 적용될 수 있을 것으로 기대가 되고 있다.


6. 결론
최근 바이오센서 기술은 반도체 기반 나노 기술의 진화와 생명공학 기술의 눈부신 발전 아래 비약적인 기술 성장을 이뤄내고 있다.
다양한 바이오센서 중 반도체 트랜지스터 소자인 FET을 소자화하여 생물학적 신호를 전기적 신호로 보다 민감하게 검출할 수 있게 되었다.
또한 최근에는 우수한 전기적 성질을 갖는 나노 재료를 응용하여 기존 생물학적 분자량이 큰 바이러스나 박테리아, 당뇨 진단 등의 범위를 넘어 분자량이 아주 작은 DNA나 미세가스 검출까지 가능한 수준이 되었다.
향후에는 전기전자적 신호를 딥러닝을 통해 학습 패턴하여 검출 인식 정확도를 높이는 기술과 생물학적 단백질 수용체를 나노 물질 위에 바이오 탐침으로 형성하여 다중의 타깃 생물 분자를 선택적으로 검출하고 판단할 수 있는 인공지능화된 나노 바이오센서 기술이 주목받을 것으로 예상된다.
이를 통해 친환경, 신종 질병 등 사회적 이슈가 되고 있는 현상학적 문제를 해결하고 보다 편리한 인간의 삶에 기여할 수 있는 AI, 로봇, 빅데이터, 자율주행 등의 기술로 응용 확대될 것으로 기대된다.
7. 참고 문헌
[1] Electrochemical Biosensor ? Sensor Principles and Architectures, Dorothee Grieshaber외 2명
Sensors 2008, 8, 1400-1458
[2] Gokuraju외 1명, Advancement and Challenges of Biosensing Using Field Effect Transistors,Bisosensors 2022, 12, 647
[3] Huiping Li 외 6명, Application of Silicon Nanowire Field Effect Transistor (SiNW-FET) Biosensor with High Sensitivity, Sensors 2023, 23, 6808
[4] K. Yoo, Physics & High Technology, 16, 2 (2007)
[5] 송광섭, 2011년 3월, 전자공학회 논문지 제 48권 SC편 제 2호, 전계효과 트랜지스터 (FETs)를 이용한 전하 검출형 DNA 센서에서 Debye length에 따른 검출 감도
[6] Anouk Beraud 외 5명, Graphene field-effect transistors as bioanalytical sensor: design, operation and performance, Analyst, 2021, 146, 403-428
[7] Mohammed Sedki 외 2명, Nano-FET-enabled biosensors: Materials perspective and recent advances in North America, Biosensors and Bioelectronics 176 (2021) 112941
[8] Jeyakumar Ramanujam 외 2명, Silicon Nanowire Growth and Properties: A Review, Mater. Express, Vol. 1, No. 2, 2011
[9] Zhi-Jun Zhao, Sang-Ho Shin 외 8명, Direct Chemisorption-Assisted Nanotransfer Printing with Wafer-Scale Uniformity and Controllability, ACS Nano 2022, 16, 378-385
[10] Chi-Chang Wu, Silicon Nanowires Length and Numbers Dependence on Sensitivity of the Field-Effect Transistor Sensor for Hepatitis B Virus Surface Antigen Detection, Biosensor 2022, 12 (2), 115
[11] Xiaoxian Zhang 외 3명, Electronic Detection of Escherichia coli O157 : H7 Using Single-Walled Carbon Nanotubes Field-Effect Transistor Biosensor, Engineering, 2012, 5, 94-98
[12] Rhiannan Forsyth 외 2명, Graphene Field Effect Transistor for Biomedical Applications: Current Status and Future Prospects, Diadnostics 2017, 7, 45
[13] Giwon Seo 외 14명, Rapid Detection of COVID-19 Causative Virus (SARS-CoV-2) in Human Nsopharyngeal Swab Specimens Using Filed-Effect Transistor-Based Biosensor, ACS Nano 2020, 14, 5135-5142
[14] O. S, Kwon and J. Jang, in Bioelectronics Nose, J.H.Lim and T.H Park, Editors, Springer, Dordrecht, Chapter 13, 243 (2013)
[15] 권오석, FET 특성 기반 나노바이오센서 분석기술, 고분자 과학과 기술 제 26권 4호, 2015년 8월
[16] Tae Hyun Kim 외 6명, Single-Carbon-Atomic-Resolution Detection of Odorant Molecules using a Human Olfactory Receptor-based Bioelectronic Nose, Adv, Mater. 2019, 21, 91-94
[17] So-ong Kim 외 5명, Ni-rGO Sensor Combined with Human Olfactory Receptor-Embedded Nanodiscs for Detecting Gas-Phase DMMP as a Simulant of Nerve Agents, ACS Senss, 2023, 8, 3095-3103
바이오센서(biosensor)는 1960년대 효소 전극을 이용한 포도당을 감지한 글루코즈 센서 개발을 시작으로 1990년대 후반까지는 주로 임상적인 수요가 큰 혈당 센서에 집중되어 왔으나, 최근 바이오(BT), 정보통신(IT), 나노기술(NT), 환경 및 에너지 (ET) 등 기술간 융합으로 새로운 패러다임가능성을 보여주고 있다.
특히 급속도로 성장 중인 생명공학과 반도체 기술 기반의 IT 나노기술이 만난 NBIT 융복합 기술은 유전자 치료, 줄기세포 기술, 암 정복 등 여러 형태로 응용 발전하고 있다. 이 중 나노 바이오센서는 다양한 질병의 검사, 치료, 예후 모니터링이 필요한 임상진단 분야에서 비약적인 기술 개발 및 응용 가능성을 제시하고 있다.
.JPG)
글/ 고려대학교 주병권 교수님 연구실
주병권 (고려대학교 전기전자공학부 교수)
김기수 (고려대학교 전기전자공학부 박사 과정)
목차
1. 서론
2. FET 나노 바이오센서 원리
3. Debye 길이
4. 성능 향상을 위한 나노 재료 기술
4-1. SiNW (실리콘 나노와이어)
4-2. CNT (탄소 나노튜브)
4-3. Graphene (그래핀)
5. FET 나노 바이오센서 연구 동향
5-1. COVID-19 나노 바이오센서
5-2. 나노 바이오 전자 코
6. 결론
7. 참고 문헌
1. 서론
나노 바이오센서는 특정 물질에 인식/반응하는 바이오 탐침(bio-probe)이 전기/화학/광학적 변환기(transducer)와 결합하여 타깃 생물분자와의 상호작용을 통해 극미량의 생화학적 물질을 선택적으로 감지할 수 있는 소자를 뜻한다.
생물학적 탐침은 압타머(aptamer), 항원/항체(antigen), 수용체(receptor), 베지클(vesicle) 등이 있으며 변환기는 전도성 나노 구조체(CNT, 전도성 고분자, SiNW, 그래핀, TMD 등)와 형광 구조체(금속, 퀀텀닷), 나노 에너지 상향물질(up-conversion) 등이 있다(그림 1).

그림 1. 바이오 센서의 구성 [1]
나노 바이오센서는 변환기 종류에 따라 크게 기계/광/전기화학/전기적 소자로 구분할 수 있으며(그림 2), 특히 전기적 신호를 감지하는 반도체 기술 기반 FET(전계유발효과 트랜지스터, Field-effect transistor)의 경우 소형화, 대량생산, 고민감도, 고속도 진단이 가능하다는 점에서 매우 큰 장점을 갖고 있다. 본 기고에서는 바이오센서 기술의 원리 및 다양한 나노 재료 기술을 이용한 고민감도/고속 검출 바이오센서 소자 개발에 대해 다루고자 한다.

그림 2. 작동 방식에 따른 다양한 바이오센서 종류
2. FET 나노 바이오센서 원리
일반적인 반도체 센서 MOSFET은 소스(source), 드레인(drain), 게이트(gate)로 구성되어 있다. 이러한 구조에서 게이트에 양의 전압, 소스에 음의 전압이 걸리게 되면 표면전자 축적으로 N채널이 형성된다. 그러나 게이트와 소스 사이에 음의 전압이 걸리거나 전압이 걸리지 않을 경우 이 N채널은 사라지게 된다. 이렇게 선택적으로 형성되는 N채널을 통하여 소스와 드레인 사이 선택적으로 전류가 흐르기 때문에 게이트 전압은 소자 내 흐르는 전류를 제어하게 된다.
이와 유사하게 FET 나노 바이오센서는 전하를 띤 타깃 생물분자와 바이오 탐침이 결합할 때 표면 전위 변화가 발생될 수 있다. 이 전위 변화는 N채널을 형성하거나 소실시키는 기존 MOSFET에서의 게이트 전압 역할과 같으며 이로 인해 소스에서 드레인으로 흐르는 전류값 변화가 유도될 수 있다(그림 3).
 그림 3. FET 소자와 FET 나노 바이오 소자의 구조 비교
그림 3. FET 소자와 FET 나노 바이오 소자의 구조 비교바이오센서의 검출 동작은 3단계로 구성된다. 첫째, 타깃 생물분자를 인지하는 단계로써 생물분자의 농도에 따른 전도도의 변화값을 유도한다. 둘째, 바이오 탐침이 인지한 전기적 성질 변화가 전기적 신호로 전환된다. 셋째, 전환된 전기적 신호를 증폭하여 데이터로써 처리한다 (그림 4).
이 때 타깃 생물분자는 나노 전도성 물질(채널)까지 확산 이동 후 화학적/물리적 흡착(반데르 발스 힘)을 하게 되며 이로 인해 전환되는 전기적 신호는 전도도 변화, 문턱전압 변화, 유도되는 전류값의 변화를 의미한다.

그림 4. 바이오센서의 검출 동작 및 검출 원리 [2]
반도체 소자인 FET의 종류와 흡착되는 타깃 생물분자의 전하 종류에 따라 그림 5와 같은 형태로 전류값의 변화가 발생된다.
또한 그림 6에서 보는 바와 같이 문턱 전압이나 전도도 값의 변화로 검출 신호를 읽을 수도 있다.

그림 5. FET 소자 종류 및 타겟 생물분자의 종류에 따른 검출 신호 변화 [3]
 P타입 CNT 기반 FET 나노 바이오센서의 특성, (b) 문턱전압 변화, (c) 전도도 변화.jpg)
그림 6. (a) P타입 CNT 기반 FET 나노 바이오센서의 특성, (b) 문턱전압 변화, (c) 전도도 변화 [4]
3. Debye 길이
FET 바이오센서는 전해질이 존재하는 용액 내 반도체 소자가 담겨 있는 형태로 작동한다. 따라서 이온 농도가 높은 용액 속에서 동작을 하게 된다면 용액 속의 이온이 전기적 신호를 상쇄(neutralization)시킴으로써 FET의 전기적 변화 측정이 어려워질 수 있다.
이러한 전기적으로 차폐되는 정도를 표현하는 개념을 Debye 길이라고 하며, 전하를 띠고 있는 입자가 영향을 미치는 거리를 의미한다. Debye 길이에 대한 Helmholtz, Gouy, Chapman, Stern 등 다양한 모델이 제시되어 왔으며 결론적으로 Debye 길이 K는 이온의 농도가 증가할수록 감소하게 된다 [5], [6].
즉, 이온 농도에 따라 결정되는 전하간 유효거리인 Debye 길이는 고농도 이온에 의한 중성화로 전기적 시그널이 약화되어 FET 바이오센서의 민감도가 저하될 가능성이 높아 기능적인 설계가 요구된다(그림 7). 이러한 문제를 해결하기 위해 바이오 탐침 길이 감소(인공항체, 앱타머 등), 저농도 용액 사용, 용액 탈양성자화 및 PH 증가, 고주파 처리법 등 다양한 연구가 적용되고 있다.

그림 7. Debye 길이 모델링 및 FET 나노 바이오센서 소자에 적용된 모사 설계도 [5]
4. 성능 향상을 위한 나노 재료 기술
기존의 박막 형태의 FET 바이오센서의 경우 박막 트랜지스터 표면과 타깃 생물분자간 반응을 통한 트랜지스터 전류 변화를 측정하는 방식이었지만, 이러한 박막 트랜지스터의 경우 크기가 작아지면 반응 표면적이 감소하여 센서의 민감도가 급격하게 떨어진다는 단점을 갖고 있었다.
따라서 박막을 반응 표면적이 넓은 나노 물질로 대체함으로써 고민감도 초소형 바이오센서를 제작할 수 있다는 가능성이 제기되었다. 이는 생체분자의 작은 크기가 나노 구조체와 유사하다는 점과 나노 물질의 부피당 생체분자와 결합할 수 있는 표면적이 크게 향상되기 때문이다 (그림 8).
또한 나노 물질 재료 자체의 높은 전기전도도 및 전하 이동도를 통해 센서 성능 지표인 검출 한계(LOD, Limit of detection)을 개선시킬 수 있다 [7]. 추가적으로 나노 물질의 형상 및 구조 변경과 나노 물질의 화학적 표면 기능화를 통해 다양한 연구 활동이 진행되고 있으며, 본 고에서는 최근 가장 활발히 발표되고 있는 대표적인 나노 물질에 대해서 다뤄보고자 한다.

그림 8. FET 나노 바이오 센서에 적용되는 0D, 1D, 2D 나노 물질 재료 [7]
4-1. SiNW (실리콘 나노와이어)
SiNW는 일반적으로 랜덤한 방향과 직경 길이로 성장하지만 성장 방법 및 공정을 조절하여 다양한 형태로 제어 가능하다. 따라서 SiNW의 전기적 특성은 성장 방향, 직경, 표면 개질, 도핑 및 와이어의 정렬 방향에 영향을 받게 된다. 예를 들어 SiNW의 밴드갭은 나노와이어의 직경에 반비례한다. 또한 2011년 Ramanujam 그룹에서는 SiNW의 전하 이동도(Charge mobility)와 합성 및 구조와의 관계를 이론적 모델과 실험 결과를 통해 밝힌 바 있다 [8]. 캐리어 이동성은 도핑, 열처리 및 산화물 결함의 패시베이션에 의해 개선됨을 보고한 바도 있다.
일반적으로 실험 결과를 통해 SiNW의 직경, 길이, 개수가 감소할수록 센서의 민감도 및 감지속도가 빨라지는 경향을 보였으며, 단위 부피당 표면적비 증가를 통한 표면 전하 효과와 전자 이동속도 증가와 관계된다고 확인되었다.
직경이 20 nm로 작은 SiNW의 경우 열처리 공정을 통해 최대 103 cm2V-1s-1 수준의 전하 이동도를 보이며, 직경이 5 nm 이하로 형성된 경우 전자와 홀의 이동도는 약 325 cm2V-1S-1와 750 cm2V-1s-1 수준까지 확인되었다. 또한 SiNW 나노 물질은 높은 전류 on/off 비, 낮은 누설전류 특성은 물론 도핑, 표면, 와이어 디자인을 설계함으로써 다양한 전기적 특성을 제어할 수 있다는 점에서 나노 바이오센서 재료로 선호되고 있다.
SiNW 나노 물질은 고가이지만 정확하고 균일한 합성과 패터닝이 가능한 Top-down (하향식) 리소그래피와 저가 대량 생산이 가능하지만 불균일한 합성이 이루어지는 Bottom-up (상향식) 기체-액체-고체(VLS) 공법을 통해 제조가 가능하다. 최근에는 보다 진보된 나노 임프린트 기술을 이용하여 대량 생산 가능하면서도 균일한 SiNW 구조를 형성시키는 신규 공법이 소개되고 있다(그림 9).

그림 9. SiNW 성장 방식 비교 [9]

그림 10. SiNW가 형성된 FET 소자의 SEM 이미지 [10]
4-2. CNT (탄소 나노튜브)
CNT는 6개의 원자로 이루어진 고리로 탄소 간 결합은 sp2 구조를 갖는다. 이 그래핀 시트 (graphite sheet)가 원통형으로 말려 있는 구조로 카이랄(말림) 지수에 따라 전기적 특성은 반도체 및 도체의 특성으로 구분될 수 있으며 구리의 103배(~10^7 S/m)의 매우 높은 전기전도도(~3,500 W/mK)와 다이아몬드 수준의 열전도도를 갖게 된다. CNT는 직경이 1~30 nm, 길이는 수~수백 um로 매우 높은 종횡비를 가지며 넓은 표면적(50~1,315 m2/g)으로 센서 감도를 향상시킬 수 있다는 장점을 갖는다.
또한 금속보다 우수한 100 GPa 수준의 인장강도와 수 TPa 수준의 탄성계수를 갖고 있기 때문에 유연성 소자로도 적용이 용이하기 때문에 FET 나노 바이오센서로 매우 적합한 나노 물질이다.
 SWCNT의 다양한 카이랄 특성, (b) 다양한 카이랄 특성으로 구성된 MWCNT 구조.jpg)
그림 11. CNT 구조 및 카이랄 특성 (a) SWCNT의 다양한 카이랄 특성, (b) 다양한 카이랄 특성으로 구성된 MWCNT 구조 [7]
이러한 CNT 나노 물질은 FET 나노 바이오센서에 적용하기 위해 필름의 형태로 제작하여 소자에 전사하게 된다. 우선 CNT를 성장시킨 후 정제, 분산, 분리, 도핑 등의 공정이 필요하다.
CNT는 아크 방전, 레이저 열처리, 화학기상증착(CVD) 등을 통해 성장시킨 후 카본계 불순물 및 촉매 금속 불순물 등을 제거하기 위한 산 처리와 고온 열처리를 통해 정제를 함으로써 보다 고순도의 CNT를 얻어 낼 수 있다. 이후 CNT간 반데르발스 힘으로 결합된 번들을 분리하기 위해 볼밀링, 초음파 처리, 계면활성제, 화학적 산화처리를 통해 분산을 시키게 된다. 이렇게 형성된 CNT는 앞서 설명한 바와 같이 카이랄 특성으로 인한 반도체성과 금속성이 혼재되어 있는 상태이기 때문에 밀도차이를 이용한 초원심분리기나 칼럼 크로마토 공정을 통해 선택적으로 분리가 필요하다.
마지막으로 확산로를 통한 합성 혹은 도펀트가 포함된 폴리머를 이용하여 전자를 공급함으로써 CNT의 전기적 특성을 조절할 수 있다. 이렇게 형성된 CNT는 딥 코팅, 스프레이 코팅, 잉크젯 코팅 등 다양한 방법을 통해 소자 위에 전사함으로써 CNT 기반 FET 나노 바이오센서를 제작하게 된다(그림 12).
이렇게 제작된 FET 바이오센서의 경우 CNT의 우수한 물성으로 인해 전기 전도성이 우수하고, 고집적도, 저전력, 빠른 스위칭 속도 등의 장점을 가지고 있으나 CNT 배열, 카이랄 특성 기인 도체/반도체성 CNT 분리, CNT 특성 균일도, 전극/CNT간 오믹컨택 등의 물성 및 공정 이슈가 존재하여 향후 개선이 필요한 상황이다.

그림 12. CNT 필름이 전사된 FET 나노 바이오센서의 SEM 이미지 [11]
4-3. Graphene (그래핀)
그래핀은 탄소 동소체 중 하나로 탄소 원자들이 모여 sp2 공유결합으로 2차원 평면 구조를 이루고 있다. 각 탄소 원자들은 육각형의 격자를 이루며 육각형의 꼭지점에 탄소 원자가 위치하고 있는 모양이다. 그래핀은 실리콘의 100배 수준의 높은 전하 이동도와 높은 비표면적 (2,630 m2/g)을 갖고 있어 나노 센서로써 매우 우수한 민감도를 확보할 수 있는 물질이다.
또한 높은 열전도도(구리의 13배), 전류 밀도(구리의 100배) 및 내화학성, 기계적 강도, 유연성, 투명성의 장점도 갖고 있다. 하지만 물질 내부에 밴드갭이 없는 제로 밴드갭 특성으로 인해 인위적 도핑 공정이 필요하고 이 과정에서 우수한 전기적 특성이 저해된다는 점과 낮은 전류 스위칭 비로 인해 센서 감도의 저하를 가져올 수 있다는 문제점도 있다. 소자를 제작하는 과정에서 그래핀의 산화도 발생할 수도 있다(그림 13).
따라서 이러한 이슈들을 개선해 나가기 위해 최근 그래핀 계면 및 결함 제어, 산화/ 환원 그래핀 기반 설계, 그래핀 폭을 좁게 만드는 나노 리본 구조 형성, 전류 채널을 새롭게 설계하는 기술 등이 제시되고 있다.
 특성 및 제로 밴드갭 형태의 그래핀 구조.jpg)
그림 13. 디락 (Dirac) 특성 및 제로 밴드갭 형태의 그래핀 구조 [12]
이러한 그래핀 나노물질은 FET 나노 바이오센서에 적용하기 위해 합성, 정제, 분산, 분리/전사 공정 후 도핑처리를 하게 된다. 그래핀을 제조하는 방식은 첫째, 흑연으로부터 그래핀을 만들어 내는 Top-down 방식과 둘째, 탄소원으로부터 그래핀을 화학적으로 합성하는 Bottom-up 방식이 있다.
구체적으로는 스카치 테이프를 이용하여 물리적으로 벗겨 내는 기계적 박리법 및 화학적 박리법, 화학기상 증착법(CVD 증착), 결정 성장법(Epitaxial growth) 등 다양한 방법들이 있으나 최근 고품질의 그래핀을 대량생산하는데 장점이 있는 화학기상 증착법을 개발하여 상용화 준비를 하고 있는 연구 기관 및 업체들이 나타나고 있다(그림 14).
마지막으로 이렇게 형성된 그래핀은 필름의 형태로 FET 나노 바이오센서 소자 위에 전사되는데 가장 대표적인 방식은 Ni이나 Cu 금속 호일 위에 성장/형성된 그래핀을 화학 에칭하여 전사하는 공정이라고 할 수 있다.

그림 14. 합성된 그래핀 필름을 FET 나노 바이오센서 소자 위에 전사한 SEM 이미지
이와 같이 다양한 나노 재료와 구조들이 FET 나노 바이오센서에 적용되고 있으며 그림 15와 같이 각각의 특성과 연구방향을 정리해 보았다.

그림 15. 다양한 나노 물질 재료의 특성 비교 및 연구 방향
5. FET 나노 바이오센서 연구동향
5-1. COVID-19 나노 바이오 센서
최근 코로나 팬더믹 시대를 맞아 매우 다양한 바이러스 검출을 위한 센서 개발이 이뤄졌다.
이 중 한 예로써 높은 비표면적과 빠른 전자 이동도를 가진 그래핀 나노 물질을 FET 나노 바이오센서에 적용하여 COVID-19(코로나 바이러스)를 검출한 바 있다.
그래핀 시트에 COVID-19와 항원체와 특정 결합할 수 있는 항체를 코팅하고, 그래핀과 이 항체간 계면을 고정화하기 위해 계면 결합제(링커)로써 PBASE (1-pyrenebutyric acid N-hydroxysuccinimide ester)를 사용하였다. 이를 통해 COVID-19 감염 여부를 고민감도로 검출할 수 있었으며 센서의 성능 지표인 검출한계(LOD)가 약 펨토몰(~ fm) 수준으로 매우 높은 결과를 확인할 수 있었다(그림 16).
 COVID-19 검출용 FET 나노바이오 센서 플랫폼, (b) PBS내에서 COVID-19 항원에 대한 바이오 센서 검출 결과, (c) COVID-19 항원 주입량에 따른 결과값 (Vds = 0.01V), (d) COVID-19와 MERS-CoV 바이러스간 선택적 검출 반응.jpg)

그림 16. (a) COVID-19 검출용 FET 나노바이오 센서 플랫폼, (b) PBS내에서 COVID-19 항원에 대한 바이오 센서 검출 결과, (c) COVID-19 항원 주입량에 따른 결과값 (Vds = 0.01V), (d) COVID-19와 MERS-CoV 바이러스간 선택적 검출 반응 [13]
5-2. 나노 바이오 전자 코 (Bioelectric-Nose)
전자 코는 냄새를 구성하는 화학물질을 정량적으로 센싱하고 감지하는 장치로써 바이오, 식품, 군사 산업 등 다양한 분야에 활용되고 있다. 1970년대부터 인간의 호기 가스(Breath gas)를 분석하기 위해 기술 개발이 시작되었으나, 수 백 가지 종류의 호기 가스를 선택적으로 민감하게 센싱하는데 극히 제한적이었다.
이러한 문제점을 극복하기 위해 최근에는 사람의 코를 모방한 나노 바이오 전자 코를 개발하고 있다. 사람의 코는 약 400여개의 바이오 탐침(후각 수용체)를 가지고 있으며 각각의 바이오 탐침들이 하나의 냄새 분자들과 선택적/특이적으로 결합함으로써 냄새를 지각하게 된다.
따라서 특정 냄새분자와 결합 가능한 바이오 탐침과 FET 나노 센서를 융복합함으로써 기존의 수백~수천 배가 넘는 센싱 민감도와 특이도를 확보할 수 있었다. 전자 코 또한 FET 나노 바이오센서와 같이 바이오 탐침(후각 수용체)와 특정 냄새분자가 결합될 때 형성된 게이트 전압의 값에 따라 트랜지스터 소자의 표면 전하량이 변화되는 원리를 따른다(그림 17).

그림 17. 그래핀 FET 나노 바이오 전자 코의 냄새분자 검출 메커니즘 [14], [15]
탄소 나노튜브(CNT)를 FET 나노 센서에 적용하고, 바이오 탐침에 필요한 단백질체를 대장균 시스템을 통해 생산 후 CNT 채널에 고정화한 결과 화학적 구조가 유사한 특정 냄새 분자만을 선택적을 검출할 수 있었음을 확인하였다 (그림 18).
또한 MEMS 공정을 이용한 그래핀 마이크로 패턴된 FET 나노 바이오 센서를 제작하여 여러가지 종류의 냄새 분자를 동시다발적으로 측정하는 플랫폼 또한 보고된 바 있다. 이 연구에서는 특히 화학무기의 한 종류인 사린 가스(독가스) 감지를 위해 사린 가스와 유사한 구조이나 독성이 적은 디메틸 메틸포스포네이트(DMMP)로 대체하고, 바이오 탐침인 hOR2T7을 그래핀에 구조화하는 형태로 검출하였다. 이는 인체 단백질인 바이오 탐침이 안정적으로 타겟 냄새 분자와 결합할 수 있도록 세포막을 감싸고 지지하는 형태로 구조화함으로써 민감도와 특이도를 개선시킬 수 있기 때문이다(그림 19).
이와 같은 나노 바이오 전자 코 기술은 현재 화장품, 식료품 등에 적용되고 있는 상황이지만 향후에는 사람의 호흡 가스로부터 방출되는 질병(폐암, 유방암 등 암, 알츠하이머, 당뇨 등)이나 바이러스, 기타 마약류나 독성 가스 혹은 친환경(공기 질) 기술 등에 활발히 적용될 수 있을 것으로 기대가 되고 있다.

그림 18. (a) CNT 기반 바이오 전자 코 플랫폼, (b) 다종 냄새 분자 중 선택적 검출된 결과 [15], [16]

그림 19. (a) 사린 가스와 결합하는 후각 수용체 단백질인 hOR2T7을 그래핀에 코팅한 니켈과 결합한 나노 바이오 전자 코 플랫폼, (b) 사린 가스 농도에 따른 사린 가스 검출, (c) 다른 냄새 분자와 선택적 검출된 결과 [17]
6. 결론
최근 바이오센서 기술은 반도체 기반 나노 기술의 진화와 생명공학 기술의 눈부신 발전 아래 비약적인 기술 성장을 이뤄내고 있다.
다양한 바이오센서 중 반도체 트랜지스터 소자인 FET을 소자화하여 생물학적 신호를 전기적 신호로 보다 민감하게 검출할 수 있게 되었다.
또한 최근에는 우수한 전기적 성질을 갖는 나노 재료를 응용하여 기존 생물학적 분자량이 큰 바이러스나 박테리아, 당뇨 진단 등의 범위를 넘어 분자량이 아주 작은 DNA나 미세가스 검출까지 가능한 수준이 되었다.
향후에는 전기전자적 신호를 딥러닝을 통해 학습 패턴하여 검출 인식 정확도를 높이는 기술과 생물학적 단백질 수용체를 나노 물질 위에 바이오 탐침으로 형성하여 다중의 타깃 생물 분자를 선택적으로 검출하고 판단할 수 있는 인공지능화된 나노 바이오센서 기술이 주목받을 것으로 예상된다.
이를 통해 친환경, 신종 질병 등 사회적 이슈가 되고 있는 현상학적 문제를 해결하고 보다 편리한 인간의 삶에 기여할 수 있는 AI, 로봇, 빅데이터, 자율주행 등의 기술로 응용 확대될 것으로 기대된다.
7. 참고 문헌
[1] Electrochemical Biosensor ? Sensor Principles and Architectures, Dorothee Grieshaber외 2명
Sensors 2008, 8, 1400-1458
[2] Gokuraju외 1명, Advancement and Challenges of Biosensing Using Field Effect Transistors,Bisosensors 2022, 12, 647
[3] Huiping Li 외 6명, Application of Silicon Nanowire Field Effect Transistor (SiNW-FET) Biosensor with High Sensitivity, Sensors 2023, 23, 6808
[4] K. Yoo, Physics & High Technology, 16, 2 (2007)
[5] 송광섭, 2011년 3월, 전자공학회 논문지 제 48권 SC편 제 2호, 전계효과 트랜지스터 (FETs)를 이용한 전하 검출형 DNA 센서에서 Debye length에 따른 검출 감도
[6] Anouk Beraud 외 5명, Graphene field-effect transistors as bioanalytical sensor: design, operation and performance, Analyst, 2021, 146, 403-428
[7] Mohammed Sedki 외 2명, Nano-FET-enabled biosensors: Materials perspective and recent advances in North America, Biosensors and Bioelectronics 176 (2021) 112941
[8] Jeyakumar Ramanujam 외 2명, Silicon Nanowire Growth and Properties: A Review, Mater. Express, Vol. 1, No. 2, 2011
[9] Zhi-Jun Zhao, Sang-Ho Shin 외 8명, Direct Chemisorption-Assisted Nanotransfer Printing with Wafer-Scale Uniformity and Controllability, ACS Nano 2022, 16, 378-385
[10] Chi-Chang Wu, Silicon Nanowires Length and Numbers Dependence on Sensitivity of the Field-Effect Transistor Sensor for Hepatitis B Virus Surface Antigen Detection, Biosensor 2022, 12 (2), 115
[11] Xiaoxian Zhang 외 3명, Electronic Detection of Escherichia coli O157 : H7 Using Single-Walled Carbon Nanotubes Field-Effect Transistor Biosensor, Engineering, 2012, 5, 94-98
[12] Rhiannan Forsyth 외 2명, Graphene Field Effect Transistor for Biomedical Applications: Current Status and Future Prospects, Diadnostics 2017, 7, 45
[13] Giwon Seo 외 14명, Rapid Detection of COVID-19 Causative Virus (SARS-CoV-2) in Human Nsopharyngeal Swab Specimens Using Filed-Effect Transistor-Based Biosensor, ACS Nano 2020, 14, 5135-5142
[14] O. S, Kwon and J. Jang, in Bioelectronics Nose, J.H.Lim and T.H Park, Editors, Springer, Dordrecht, Chapter 13, 243 (2013)
[15] 권오석, FET 특성 기반 나노바이오센서 분석기술, 고분자 과학과 기술 제 26권 4호, 2015년 8월
[16] Tae Hyun Kim 외 6명, Single-Carbon-Atomic-Resolution Detection of Odorant Molecules using a Human Olfactory Receptor-based Bioelectronic Nose, Adv, Mater. 2019, 21, 91-94
[17] So-ong Kim 외 5명, Ni-rGO Sensor Combined with Human Olfactory Receptor-Embedded Nanodiscs for Detecting Gas-Phase DMMP as a Simulant of Nerve Agents, ACS Senss, 2023, 8, 3095-3103
<저작권자(c)스마트앤컴퍼니. 무단전재-재배포금지>
본 기사의 전문은 PDF문서로 제공합니다.
(로그인필요)
다운로드한 PDF문서를 웹사이트, 카페, 블로그등을 통해 재배포하는 것을 금합니다. (비상업적 용도 포함)
다운로드한 PDF문서를 웹사이트, 카페, 블로그등을 통해 재배포하는 것을 금합니다. (비상업적 용도 포함)
100자평 쓰기